¿Por qué la sal derrite el hielo?

El hielo es uno de los 3 estados naturales del agua, no es otra cosa que agua sólida cristalizada, congelada. El agua pura a la altitud del nivel del mar se congela a 0 ºC y la densidad del hielo a esta temperatura es de 0,9169 gr/cm3. Mientras que la mayoría de las sustancias se contraen al congelarse, el agua es una de las pocas sustancias que al congelarse aumenta de volumen, o lo que es igual disminuye su densidad. Este hecho evita que las regiones polares de la Tierra se congelen en toda su superficie, ya que el hielo flota en el agua y es lo que queda superficialmente expuesto a los cambios de temperatura.
Cuando el hielo y el agua están en contacto, las moléculas de la superficie de hielo se funden en el agua (fusión), y las moléculas de agua son capturados en la superficie del hielo (congelación). Cuando la cantidad de congelación es la misma que la de fusión, el hielo y el agua están en equilibrio dinámico entre sí. El equilibrio entre la congelación y el deshielo se puede mantener a 0 ºC, el punto de congelación del agua, a menos que cambien las condiciones de una forma que favorezcan un proceso u otro. Este equilibrio se rompe fácilmente por efecto de la temperatura, si aumentamos la temperatura favorecemos la fusión y si esta desciende se favorece la congelación.
El descenso crioscópico y la sal
Pero este equilibrio dinámico también se rompe al añadir sal. Cuando añadimos sal al hielo lo que se funde no es el hielo sino una mezcla de hielo y sal. Cuando la sal NaCl (Na+, Cl–) entra en contacto con el hielo, los iones se combinan con las moléculas altamente polares del agua (H2δ+, Oδ–) y forman un compuesto (H2O).(NaCl). Esta mezcla tiene un punto de congelación inferior a 0º C y es la base de la aplicación de hielo en las carreteras. El descenso crioscópico es la reducción del punto de fusión de un disolvente puro que se consigue por la presencia de solutos.
¿Cualquier sustancia extraña nos permitiría rebajar el punto de congelación?. Pues si, por cada mol de partículas extrañas disueltas en un kilo de agua, el punto de congelación baja en aproximadamente 1,7-1,9 ° C. Podríamos añadir azúcar, alcohol, u otras sales que también bajaríamos el punto de congelación y derretiríamos el hielo. El descenso crioscópico es directamente proporcional a la molalidad o cantidad de soluto por kilo de disolvente.
La proporción de sal
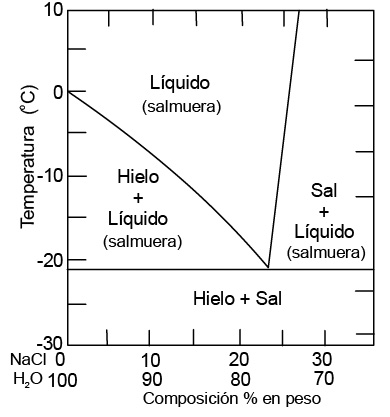 Existe una proporción de sal en agua que se comporta como si fuera una sustancia pura, técnicamente es lo que se califica como «eutéctica», que en el caso de la sal es de un 23% de sal en masa. La temperatura de fusión de esta sustancia eutéctica es de alrededor de –21 °C. Esta proporción de sal en agua es la concentración ideal con la que conseguiríamos la menor temperatura de congelación. Tanto si la proporción de sal es inferior como si es superior a esta cantidad la temperatura de congelación es superior (entre –21 °C y 0 °C). Esto lo vemos claramente en el diagrama de fase que representa la temperatura de fusión en función de las proporciones sal-agua.
Existe una proporción de sal en agua que se comporta como si fuera una sustancia pura, técnicamente es lo que se califica como «eutéctica», que en el caso de la sal es de un 23% de sal en masa. La temperatura de fusión de esta sustancia eutéctica es de alrededor de –21 °C. Esta proporción de sal en agua es la concentración ideal con la que conseguiríamos la menor temperatura de congelación. Tanto si la proporción de sal es inferior como si es superior a esta cantidad la temperatura de congelación es superior (entre –21 °C y 0 °C). Esto lo vemos claramente en el diagrama de fase que representa la temperatura de fusión en función de las proporciones sal-agua.
¿Por qué sal en las carreteras?
La sal se utiliza en las carreteras y caminos, simplemente porque es barata y fácilmente disponible. Sin entrar a valorar la eficacia de la sal frente a otros productos que en cualquier caso también dependerá de la granulometría, de los métodos de reparto, del tipo de asfalto de la carretera, etc. existe un debate importante en cuanto a la repercusión ecológica del uso masivo de este producto en nuestras carreteras . La sal se diluye en agua y ésta corre por ríos, acuíferos y demás, y además se cuestiona que repercursiones tendrá su uso a largo plazo.
En ciudades de centroeuropa se ha comprobado como su utilización producía daños en la mayoría de los árboles de estas ciudades. Además de la corrosión que provoca a los vehículos su utilización en las carreteras. Ahora, bien es verdad que en Canadá se prohibió y los accidentes de tráfico se dispararon.
Se está planteando como alternativa, principalmente la utilización de arenas, cenizas o gravillas que tienen la ventaja de ser más biodegradables y con una eficiencia similar a menor coste. ya que logran sin dañar el ecosistema derretir el hielo sobre las calles en un plazo similar de tiempo.
El hielo negro y el hielo azul
De momento la efectividad y economía de la sal hace que lo utilicemos masivamente en las situaciones invernales como la que estamos viviendo. Pero además de vez en cuando oimos hablar de términos que no dejan de ser paradojicos: lluvia helada, hielo negro, hielo azul. etc.
Algunas veces podemos ver, sobretodo en fotos de icebergs flotando en una mar helado como si todo el bloque fuera azul. Habitualmente las pequeñas burbujas de aire que quedan atrapadas en el hielo reflejan la luz, multiples veces y de todos los colores, de modo que la luz que recibimos es luz blanca. El hielo aparece azul cuando es muy consistente y las burbujas de aire no impiden el paso de la luz a través de él. Es la longitud de onda del color azul la que no es absorbida por el bloque y la que nos da la sensación de que el hielo es azul.
Pero en nuestras carreteras una de las grandes preocupaciones es el hielo negro ya que es un fenómeno muy difícil de prevenir. El hielo negro es una capa delgada de hielo lo suficientemente transparente que nos permite ver la carretera que está debajo. Ésto hace que la carretera nos de la sensación de estar mojada. Suele aparecer tras varias jornadas con temperaturas frías y se forma con mucha rapidez sobre la superficie de la carretera. Las láminas, muy delgadas, pueden surgir en un tiempo mínimo de tan solo diez minutos y, al ser totalmente transparentes, se confunden con el fondo negro del asfalto y nos pasan completamente inadvertidas ya que las confundimos con charcos. Siempre que la temperatura esté por debajo del punto de congelación y la carretera parezca estar mojada, tendremos que tener un especial cuidado con el hielo negro.
Eso o quedarnos junto a una chimenea, un buen libro y….

El artículo que habla del hielo negro me va a ayudar mucho. Lo sufro con frecuencia y lo paso fatal.
Feliz año a los de «la sirena» y ser felices!
Muy interesante el artículo para aquellos que vivimos de cerca de las bajas temperaturas. El blog de la sirena nos ofrece una información profesional con un enfoque didáctico que ayuda mucho a los ciudadanos. Por ejemplo, cuando tenga hielo en la puerta de casa y en el pasillo del jardín utilizaré las cenizas de la chimenea para disolverlo.
Cada día se aprende algo. Es una suerte que alguien te ayude y te informe de cómo protegerte ante las dificultades casi cotidianas.
Gracias!!